Você sabia que existem mais microrganismos em você do que pessoas no planeta, neh? Sim! Eles dominam a Terra e não os Gatos Illuminati como se supõe por ai… Embora sabemos que esses microrganismos sejam naturais e importante para nosso funcionamento biológico, alguns deles causam problemas de saúde, como infecções, micoses, candidíase, pneumocistose, tuberculose, etc… Antibióticos e outros fármacos que combatem esses microrganismos é muito comum de serem usados, porém os nanomateriais antimicrobianos vem sendo cada vez mais aplicados contra microrganismos de forma isolada ou em conjunto com esses fármacos no combate às doenças infecciosas. Embora a aplicação contra microrganismo seja comumente citada, ainda não se tem a exatidão dos mecanismos em que esses nanomateriais agem contra bactérias e fungos.
A nanotecnologia entra nessa jogada devido à resistência que microrganismo adquirem aos antibióticos. O nanomaterial antimicrobiano mais conhecido é de longe a nanoprata. Embora sua atividade antimicrobiana seja poderosa, ela contém alguns inconvenientes em algumas aplicações, fazendo cientistas buscar novas alternativas.
Entre os materiais mais estudados se encontram os nanometálicos como a Ag e o Cu; e para os nano óxidos estão a Ag2O, ZnO, CuO, MgO, Cao e o TiO2.
Nanopartículas de prata
A prata possui um enorme potencial antimicrobiano podendo ser atribuído aos muitos mecanismos de ação contra os microrganismo (Figura 1). Entre esses mecanismos estão a habilidade de se anexar na parede da membrana celular do microrganismo – interrompendo a captação de nutrientes necessários – e a penetração da mesma, causando buracos na membrana celular ocasionando o vazamento do material celular contido no seu interior.
A nanopartícula de prata pode interagir com grupos tióis (-SH) e aminas (-NH), se ligando a estruturas enzimáticas e em bases nitrogenadas do DNA, perturbando o funcionamento biológico da célula bacteriana.
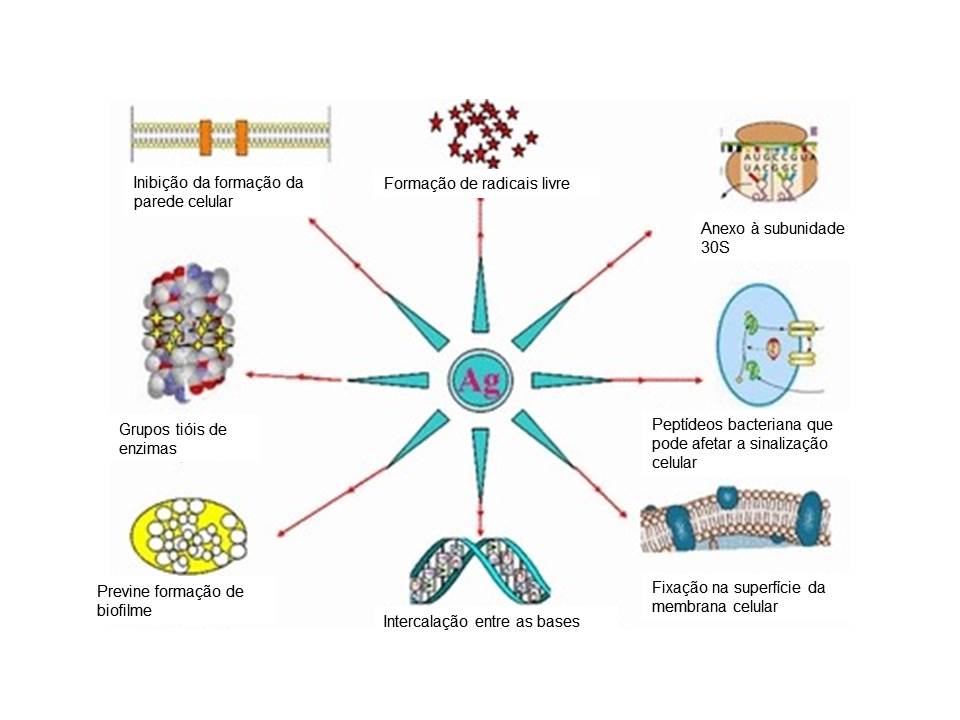
Figura 1. Os diferentes mecanismos de ação da nanoprata no controle de microrganismo
Nanopartículas de ZnO
A segurança de ZnO e a compatibilidade com a pele humana torna-a adequada como aditivo para tecido e superfície que vem entrar em contato com o corpo humano. nanopartículas de ZnO apresentam atividade antimicrobiana para bactérias Gram-positiva e Gram-negativa. A propriedade antimicrobiana de ZnO aumenta com a diminuição do tamanho de partícula, podendo em uma concentração ideal ser até mais potente que a própria nanoprata.
Nanopartículas de ZnO também são fotocatalíticas, o que contribui fortemente na sua atividade antimicrobiana. Nanomateriais fotocatalíticos geram espécies de oxigênio reativos, como os peróxidos e os radicais livres, que exterminam microrganismos. Assim como as nano ZnO, TiO2 também possui atividade fotocatalítica, agindo da mesma forma.
O mecanismo exato de ação de ZnO é ainda desconhecido, entretanto atribui-se duas possíveis propostas:
1)Geração de peróxido de hidrogênio
2)Acumulo de partícula na superfície celular da bactéria devido ás forças eletrostática.
Nanopartíulas de TiO2
Propriedade antimicrobiana do TiO2 está relacionada com a sua estrutura cristalina , forma e tamanho. O estresse oxidativo via geração de radicais livres pode ser uma particularidade importante no mecanismo para nanopartículas de TiO2 (fase anatase).
Propriedade fotocatalítica das nanopartículas TiO2 auxiliam na eficiência de erradicação bacteriana
Nanopartículas de Au
Nanopartículas de Au são não-tóxicas, possuem alta habilidade de funcionalização e efeito polivalentes.
Embora a geração de espécies de oxigênio reativas seja a principal causa de morte celular da maioria dos antibióticos e nanomateriais antimicrobianas, o Au não possui indução alguma dessas espécies.
Cui et al. provou que a atividade antimicrobiana de nanopartículas de Au são ocasionadas por:
1) a fixação destas nanopartículas à membrana bacteriana, seguida da modificação do potencial da membrana e do decréscimo do nível de ATP e
2) inibição da ligação de ARNt ao ribossomo
Estudos reportam que nanoAu funcionalizadas com 5-fluorouracil possuem maior efeito em bactérias Gram-negativas do que em Gram-positivas devido á facilidade de internalização.
Interação de cargas negativas com membrana celular que possui carga positiva.
Lima et al. reportam efeito antimicrobiano de até 95% contra E. coli e S. Typhi. Os autores relatam que a propriedade biocida foi ocasionada pela rugosidade e dispersão das nanopartículas de Au.
Nanopartículas de SiO2
Nanocompósito Ag/SiO2 possuem propriedades antimicrobianas mais potentes contra E.Coli e S. Aureus e C. Albicans enquanto que Au/SiO2 não apresentam atividade.
SiO2 atua como matriz para incorporação de nanometálicos com atividade antimicrobiana.
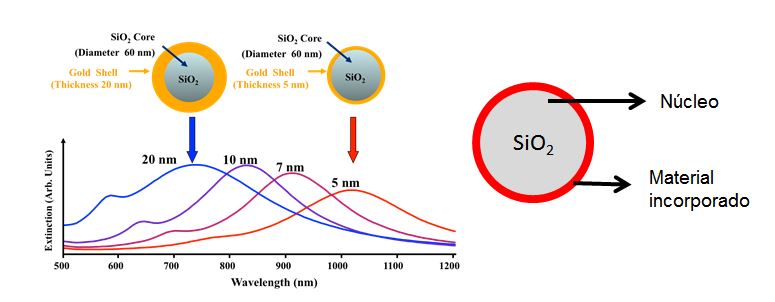
Figura 2 : Core-Shell de nanopartículas de sílica antimicrobianas.
MgO e CaO
CaO e MgO indicam forte atividade antimicrobiana relacionado à alcalinidade e espécies ativas de oxigênio.
O mecanismo é provocada pela geração de superóxido na superfície dessas partículas, e também um aumento no valor do pH pela hidratação de CaO e MgO com água.
Nanopartículas de MgO causam danos na membrana celular que consequentemente ocasionam vazamento dos conteúdos intracelular, causando a morte da célula.
Nanopartículas de MgO sozinhas ou combinadas com Nisina, um peptídio antimicrobiano, apresenta efetividade contra E. coli e Salmonela Stanley, podendo ser usadas como agente antimicrobiano em alimentos para melhorar a segurança alimentar.
Nanopartículas MgO e Cao isoladas ou em combinação são alternativas para desinfetantes com baixo custo. Isso as torna promissoras como agente antimicrobianas.
Nanopartículas de Cu e CuO
Nanopartículas de cobre possuem grande interesse para cientistas devido às suas propriedades biológicas, fisico-química e atividade biológicas a um baixo custo. Entretanto o cobre possui uma rápida oxidação quando exposta ao ar, limitando sua aplicação.
Testes com nanopartículas de CuO indicam que possuem atividade antimicrobiana. Acredita-se que as nanopartículas atravessam a membrana celular da bactéria e os danos nas enzimas vitais são gatilhos para o fator crítico nas morte celular.
Tamanho, estabilidade e concentração são fatores que contribuem para o efeito antimicrobiano. De um modo geral podem atuar de forma isolada ou incorporadas em nano ou micromateriais, como é o caso de zeólitas, que impregnadas com CuO adquiri propriedade antimicrobiana se tornando multifuncional.
Referências
Antimicrobial activity of the metals and metal oxide nanoparticles DOI: 10.1016/j.msec.2014.08.031
Antimicrobial Activity of CaO Nanoparticles DOI: 10.1166/jbn.2013.1681
Silver nanoparticles: the powerful nanoweapon against multidrug-resistant bacteria DOI: 10.1111/j.1365-2672.2012.05253.x

















 via Sol-Gel. Você faz uma solução de acetato de zinco (12,6g em 400ml de água bidestilada) e então aqueça até 50ºC. Adiciona-se 600ml de etanol absoluto
via Sol-Gel. Você faz uma solução de acetato de zinco (12,6g em 400ml de água bidestilada) e então aqueça até 50ºC. Adiciona-se 600ml de etanol absoluto 

